I. ĐỊNH NGHĨA PHẢN ỨNG OXI HOÁ – KHỬ VÀ XÁC ĐINH SỐ OXI HOÁ
1. Định nghĩa phản ứng oxi hoá – khử
Phản ứng oxi hoá – khử là phản ứng hoá học trong đó có sự thay đổi số oxi hoá của một số nguyên tố hay là phản ứng trong đó có sự chuyến electron giữa các chất phản ứng.
2. Xác định số oxi hoá trong hợp chất
Bạn đang đọc: Lý thuyết phản ứng oxi hoá – khử – http://139.180.218.5
Chú ý : Người ta ghi số oxi hoá ở phía trên nguyên tử của nguyên tố. Ghi dấu trước, số sau .
II. CHẤT KHỬ, CHẤT OXI HOÁ, SỰ OXI HOÁ, SỰ KHỬ
– Chất khử là chất nhường electron hay là chất có số oxi hoá tăng sau phản ứng.
– Chất oxi hoá là chất nhận electron hay chất có số oxi hoá giảm sau phản ứng.
(Câu thần chú: Chất khử cho tăng, chất o nhận giảm)
– Sự oxi hoá (quá trình OXH) của một chất là làm cho chất đó nhường electron hay làm tăng số oxi hoá chất đó.
– Sự khử (quá trình khử) của một chất là làm cho chất đó nhận electron hay làm giảm số oxi hoá chất đó.
* Sự nhường electron chỉ có thể xảy ra khi có sự nhận electron. Vì vậy sự oxi hoá và sự khử bao giờ
cũng diễn ra đồng thời trong một phản ứng.
* Chất khử tạo nên sự OXH, chất OXH tạo nên sự khử
III. LẬP PHƯƠNG TRÌNH PHẢN ỨNG 0XI HOÁ – KHỬ
Để lập phương trình phản ứng oxi hoá – khử theo giải pháp tháng bằng electron, ta triển khai những bước sau đây :
Bước 1 : Ghi số oxi hoá của những nguyên tố có số oxi hoá thay đổi :
Bước 2 : Viết quá trình oxi hoá và quá trình khử, cân bằng mỗi quá trình :
Bước 3 : Tìm hệ số thích hợp sao cho tổng số electron do chất khử nhường bằng tổng số electron mà
chất oxi hoá nhận .
Ví dụ:
\(F{{e}_{2}}{{O}_{3}}\,\,\,+{{H}_{2}}\,\,\,\xrightarrow{{{t}^{o}}}\,\,\,Fe\,\,\,+\,\,\,{{H}_{2}}O\)
Bước 1 : Xác định số oxi hóa, chất oxi hóa, chất khử
\(\overset{+3}{\mathop{F{{e}_{2}}}}\,{{O}_{3}}\,\,\,+\,\,\,\overset{0}{\mathop{{{H}_{2}}}}\,\,\,\,\xrightarrow{{{t}^{o}}}\,\,\,\overset{0}{\mathop{Fe}}\,\,\,\,+\,\,\,{{\overset{+1}{\mathop{H}}\,}_{2}}O\)
Chất oxi hóa : \(\overset{+3}{\mathop{Fe}}\,\) (trong Fe2O3)
Chất khử : \(\overset{0}{\mathop{{{H}_{2}}}}\,\)
Bước 2 : Viết các quá trình oxi hóa, khử
\(\overset{+3}{\mathop{F{{e}_{2}}}}\,{{O}_{3}}\,\,\,+\,\,\,2.3e\,\,\,\to \,\,\,2\overset{0}{\mathop{Fe}}\,\)
(quá trình khử)
\(\overset{0}{\mathop{{{H}_{2}}}}\,\,\,\,\,\,\,\to \,\,\,\overset{+1}{\mathop{{{H}_{2}}O}}\,\,\,\,+2.1e\)
(quá trình oxi hóa)
Bước 3 : Tìm hệ số cho hai quá trình oxi hóa và khử
Bội số chung nhỏ nhất ( BSCNN ) = 6 do đó thông số mỗi quy trình như sau :
1 \(\overset{+3}{\mathop{F{{e}_{2}}}}\,{{O}_{3}}\,\,\,+\,\,\,2.3e\,\,\,\to \,\,\,2\overset{0}{\mathop{Fe}}\,\)
3 \(\overset{0}{\mathop{{{H}_{2}}}}\,\,\,\,\,\,\,\to \,\,\,\overset{+1}{\mathop{{{H}_{2}}O}}\,\,\,\,+2.1e\)
=> Fe2O3 + 3H2 → 2Fe + 3H2O
Xem thêm: Đầu số 0127 đổi thành gì? Chuyển đổi đầu số VinaPhone có ý nghĩa gì? – http://139.180.218.5
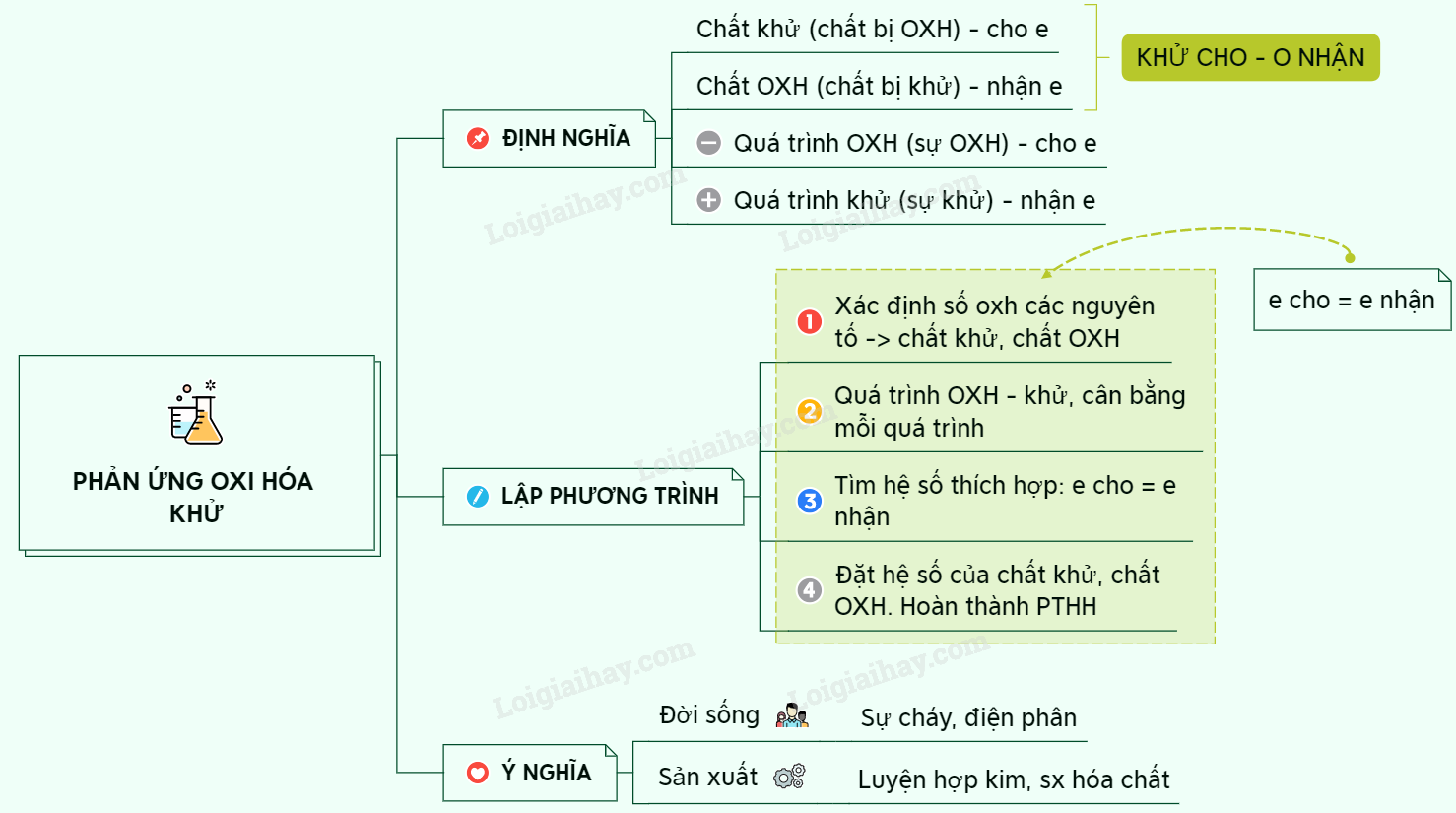
Sơ đồ tư duy: Phản ứng oxi hoá – khử
Loigiaihay.com
Source: http://139.180.218.5
Category: Thuật ngữ đời thường