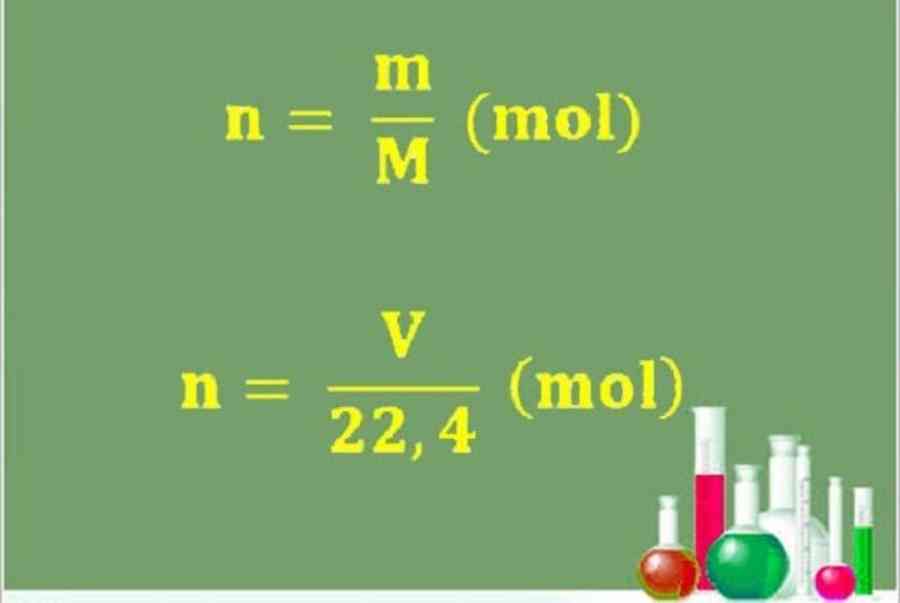Nội dung chính
Khái niệm số mol là gì?

Mol được gọi là một đơn vị đo lường cơ bản thuộc vào hệ quy chuẩn SI và được sử dụng riêng cho các hạt vĩ mô. Nó cách khác, mol chính là lượng chất có chứa số hạt đơn vị của phân tử hoặc nguyên tử chất đó. Cụ thể nó diễn tả lượng chất có chứa 6,022×10^23 số hạt đơn vị của phân tử hoặc nguyên tử chất đó.
Lưu ý, khối lượng mol của phân tử không giống khối lượng mol của nguyên tử. Ví dụ, khối lượng mol phân tử ( hydro ) là 2 g trong khi khối lượng mol của nguyên tử H ( hydro ) chỉ là 1 g .
Cách phân biệt kí hiệu :
1 mol H chỉ 1 mol nguyên tử Hidro .
1 mol H2 chỉ 1 mol phân tử Hidro .
Lịch sử phát triển của mol

Do được sử dụng thông dụng trong hóa học nên mol cũng là một trong những đơn vị chức năng có mối quan hệ mật thiết với đơn vị chức năng khối lượng nguyên tử, phân tử khối, hằng số Avogadro cũng như những khái niệm khác có trong hóa học .
Năm 1805, xuất bản bảng giá trị nguyên tử khối tương đối tiên phong trên quốc tế được nhà khoa học John Dalton ( 1766 – 1844 ) xuất bản .
Sau đó, bảng giá trị nguyên tự khối tương đối được Jöns Jacob Berzelius ( 1779 – 1848 ) khám phá và đưa ra những thông số kỹ thuật đúng chuẩn hơn .
Thế hệ tiếp theo liên tục lan rộng ra khu công trình của Berzelius phải kể tới Henri Victor Regnault ( 1810 – 1878 ), Charles Frédéric Gerhardt ( 1816 – 1856 ) và Stanislao Cannizzaro ( 1826 – 1910 ) .
Tên gọi mol Open chính thức vào năm 1894, tên này được bắt nguồn từ tiếng Đức ( molekül có nghĩa là phân tử ), do nhà khoa học Wilhelm Ostwald đặt. Trong từ điển Merriam-Webster, người ta cho rằng mol được đặt dựa theo từ gốc molekulärgewicht của tiếng Đức có nghĩa là khối lượng phân tử .
Tính đến thời gian hiện tại, mol đã được sử dụng rất phổ cập trong những nghành nghề dịch vụ tương quan đến hóa học, phân tử, nguyên tử …
Công thức tính số mol của một chất nhất định
Để tính số mol của một chất nào đó, ta sẽ vận dụng công thức sau :
n = m / M
Trong đó:
- n là số mol chất, đơn vị chức năng : mol
- M là khố lượng mol, đơn vị chức năng : g / mol
- m là khối lượng chất đó, đơn vị chức năng : g
Khố lượng mol của một chất được hiểu là khối lượng tính bằng gam của N nguyên tử hoặc phân tử của chất đó .
Khối lượng mol nguyên tử hay phân tử của một chất có cùng số trị với nguyên tử khối hoặc phân tử khối của chất đó .
Thể tích mol chất khí là gì?
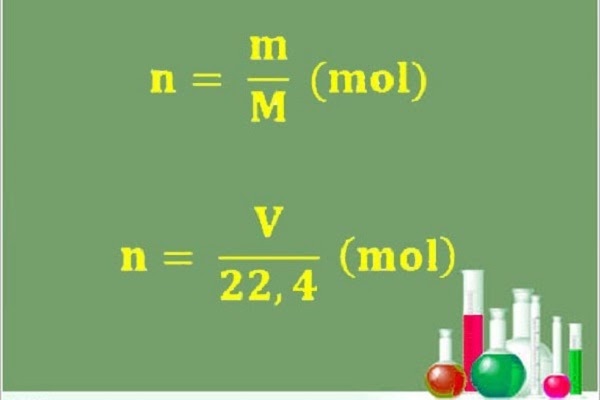
Thể tích mol phân tử của một chất khí chính là thể tích 1 mol phân tử của chất khí đó, hoặc hoàn toàn có thể là thể tích bị chiếm mới N phân tử chất đó. Trong điều kiện kèm theo nhiệt độ và áp suất không đổi khác thì thể tích mol chất khí cũng không đổi. Điều kiện tiêu chuẩn khi nhiệt độ là 0 độ C và áp suất là 1 atm thì 1 mol chất khí sẽ tương tự với thể tích 22,4 lít .
Trong điều kiện kèm theo tiêu chuẩn, những tính mol sẽ tính theo công thức sau :
n = V / 22,4
Trong đó :
- n chính là số mol
- V là thể tích khí ở điều kiện kèm theo tiêu chuẩn
- 22,4 là hằng số trong điều kiện kèm theo tiêu chuẩn .
Trong trường hợp chất khí ở trạng thái tự nhiên, không phải là điều kiện kèm theo tiêu chuẩn thì công thức trên không hề vận dụng. Chúng ta sẽ cần tới những công thức và phép tính phức tạp hơn .
Một mol của bất kì chất khí nào trong cùng điều kiện nhiệt độ, áp suất đều chiếm những thể tích bằng nhau.
Xem thêm: Đầu số 0127 đổi thành gì? Chuyển đổi đầu số VinaPhone có ý nghĩa gì? – http://139.180.218.5
Trên đây là hàng loạt những thông tin cụ thể để giải đáp vướng mắc số mol là gì. Việc nắm rõ cách tính số mol của một chất sẽ giúp bạn thuận tiện xử lý những bài toán khó. Bên cạnh đó, đây cũng chính là cơ sở để bạn thực thi tích toán khi thực thi thí nghiệm hoá học. Hy vọng rằng bạn đọc sẽ có cho mình những kiến thức và kỹ năng thật có ích .
Source: http://139.180.218.5
Category: Thuật ngữ đời thường