BS. Nguyễn Thanh Hiền
BS. Phạm Đức Đạt
Bệnh viện Nhân Dân 115
MỞ ĐẦU
Can thiệp động mạch vành qua da ( PCI ) được xem như một kế hoạch tái lưu thông mạch máu hiệu suất cao của bệnh mạch vành từ năm 1977. Nhiều điều tra và nghiên cứu lâm sàng quan trọng chứng tỏ lợi điểm của can thiệp động mạch vành qua da đã làm cho số lượng thủ pháp PCI mỗi năm ngày càng tăng đáng kể. Vào khoảng chừng 1.2 triệu ca PCI được triển khai mỗi năm ở Mỹ và khoảng chừng 2000.000 ca / năm trên toàn quốc tế. Số liệu cũng cho thấy số ca PCI tăng gấp 5 lần sau mỗi thập kỷ. So với điều trị nội khoa, PCI đã chứng tỏ giảm tỉ lệ biến chứng ở bệnh nhân NMCT cấp hay CĐTNKÔĐ rủi ro tiềm ẩn cao, cũng như làm giảm mức độ đau ngực và cải tổ chất lượng đời sống ở bệnh nhân cơn đau thắt ngực không thay đổi ( 1-4 ). Tuy nhiên không phải tái thông mạch xong là xử lý được toàn bộ và bệnh nhân không cần phải theo dõi điều trị gì. Theo Serruys P.W, sau một năm tái thông mạch, tỉ lệ bệnh nhân hết đau ngực chỉ là 78,9 % ở nhóm PCI và 89,5 % ở nhóm CABG, và tỉ lệ can thiệp lại ( đặt stent ) là 16,3 % cho nhóm PCI và 3,5 % cho nhóm CABG. Ở một nghiên cứu và điều tra khác, sau bốn năm theo dõi, tỉ lệ có CĐTN là 46 % ( 27 % CCS III-IV và 19 % CCS I-II ) cho bệnh nhân sau đặt stent. Ngoài ra, những giải pháp dự trữ thứ phát như sử dụng thuốc ức chế tiểu cầu, giảm lipid máu, ACEIs … hoàn toàn có thể giảm một cách hiệu suất cao tỉ lệ những biến cố tim mạch chính như tử trận và NMCT. Do đó làm tăng số lượng bệnh nhân sống lâu hơn, điều này hoàn toàn có thể làm tăng số bệnh nhân sau PCI ( 5,6 ). Sự ngày càng tăng này đưa đến những bác sỹ nội khoa sẽ phải đương đầu nhiều hơn với những bệnh nhân PCI. Ngoài ra, do có những văn minh mới trong PCI, nghĩa là nhiều kỹ thuật mới, cùng với nhiều biến chứng mới, sẽ gặp tiếp tục hơn. Do đó cần có những update liên tục cho những bác sỹ nội khoa về chăm nom những đối tượng người tiêu dùng bệnh nhân này. Bài viết sẽ bàn về những nguyên tắc điều trị tổng quát cũng như những yếu tố đặc biệt quan trọng trong chăm nom cho những bệnh nhân sau can thiệp mạch vành .
TUẦN ĐẦU SAU CAN THIỆP MẠCH VÀNH QUA DA
Phần lớn bệnh nhân giờ đây được xuất viện sau 24 giờ ( trong điều kiện kèm theo ở quốc tế trừ khi có biến chứng ) nếu can thiệp mạch vành qua da tinh lọc. Chăm sóc bệnh nhân xuất viện ngay lập tức tương quan tới phát hiện những biến chứng mạch máu tại chỗ, đương đầu với những biến chứng do thuốc cản quang hay do thuốc và thuyên tắc do huyết khối trong stent ( 7 ) .
Biến chứng mạch máu tại chỗ
Vị trí can thiệp mạch vành qua da hoàn toàn có thể qua động mạch đùi, động mạch quay hay động mạch cánh tay. Đường động mạch cánh tay ngày này ít dùng do năng lực gây ra những biến chứng nặng như đoạn chi do thiếu máu. Nga # động mạch đùi là đường thường dùng nhất do kỹ thuật đơn thuần, nhưng đường động mạch quay ngày càng thông dụng do năng lực trấn áp tốt biến chứng và tiện nghi cho bệnh nhân hơn. Một điều tra và nghiên cứu tổng hợp ( 8 ) gần đây cho thấy tiếp cận ngả đường quay sẽ có ít biến chứng tại chỗ hơn nhưng sẽ có tỷ suất thành công xuất sắc của thủ pháp thấp hơn do những yên cầu về kỹ thuật cao hơn .
Tần suất biến chứng của mạch máu đùi sau can thiệp mạch vành qua da đã được báo cáo giải trình vào khoảng chừng 2-6 %. Những biến chứng của đường động mạch đùi gồm có máu tụ, giả phình mạch, thông nối động tĩnh mạch, thiếu máu chi dưới, nhiễm trùng động mạch đùi và chảy máu sau phúc mạc. Tỉ lệ biến chứng phụ thuộc vào vào kích cỡ ống thông can thiệp ( < 7F sẽ ít biến chứng hơn ), mức độ kỹ thuật thực thi, tuổi ( > 65 ), giới ( nữ ), có bệnh mạch máu ngoại biên, mập phì, số lượng tiểu cầu thấp, triển khai PCI ở bệnh nhân vừa dùng thuốc tiêu sợi huyết ( can thiệp cứu vãn trong nhồi máu cơ tim cấp ), thao tác kỹ thuật của thủ thuật viên … ( 7,9,10 ) .
Biến chứng tại vị trí chọc mạch máu yên cầu phải được chẩn đoán xác lập sớm. Cần thăm khám kỹ chỗ chọc trong vài ngày vì máu tụ hoàn toàn có thể xảy ra sau tháo băng ép vài ngày bằng sờ, nghe, bắt mạch chi, siêu âm mạch máu, đôi lúc phải đo vòng đùi hàng ngày để phát hiện những trường hợp hoài nghi tụ máu trong cơ .
Máu tụ nhỏ là những biến chứng thường gặp và bộc lộ bằng những tiếng rù nhẹ và không cần phải xem xét hay điều trị đặc hiệu gì. Máu tụ lớn hay giả phình mạch xảy ra khoảng chừng 0,5 – 6,3 %. Nghi ngờ có máu tụ khi có căng vùng bẹn, sờ thấy một khối u đập, và / hoặc tiếng rù ở bẹn. Chẩn đoán xác lập bằng siêu âm. Phình nhỏ ( < 2 cm ) chỉ cần theo dõi lâm sàng và ít có rủi ro tiềm ẩn vỡ. Phình lớn điều trị bằng đè ép dưới siêu âm, tiêm thrombin dưới siêu âm, phẫu thuật, hay đặt giá đỡ có mảnh ghép phủ polyetrafluoroethylene ( polyetrafluoroethylene – covered stent – graft ). Phình quá lớn là yếu tố rủi ro tiềm ẩn vỡ động mạch do vậy phải điều trị cẩn trọng. Dò động tĩnh mạch biểu lộ bằng nghe thấy âm thổi liên tục hay đau ở vùng bẹn và cần khẳng định chắc chắn bằng siêu âm Doppler mạch. Tỉ lệ báo cáo giải trình đổi khác từ 0,2 - 2,1 %. Điều trị thì cũng tựa như như giả phình mạch. Trong những trường hợp dò và phình vẫn còn sống sót sau đè ép, hay bệnh nhân có khối máu tụ lớn hay đang lớn dần thì nên gởi bệnh nhân lại cho bác sỹ tim mạch ( 7,9,10 ) .
Xuất huyết sau phúc mạc do vị trí chọc kim quá cao trên nếp dây chằng bẹn làm cho máu hoàn toàn có thể đi vào khoang sau phúc mạc và gây đau bụng hay đau lưng mà không thấy bất kể khối máu tụ nào ở vùng bẹn. Dấu chứng cảnh báo nhắc nhở là đau kinh hoàng ở vùng sống lưng hay thắt lưng sau thủ pháp. Cũng có khi chỉ có dấu thiếu máu nặng mà không có kèm theo đau. Tần suất xuất huyết sau phúc mạc sau can thiệp mạch vành qua da là hiếm ( < 0.5 % ). Bác sỹ nên quan tâm đến xuất huyết sau phúc mạc khi có tụt huyết áp trường diễn. Tất cả những trường hợp hoài nghi xuất huyết sau phúc mạc nên cho làm CT bụng khẩn và báo lại cho bác sỹ tim mạch. Hầu hết những trường hợp hoàn toàn có thể điều trị bảo tồn bằng ngưng và / hoặc biến hóa điều trị kháng đông hay chống tiểu cầu. Chỉ dịnh phẫu thuật khi tụt HA lê dài dai dẳng với giảm hematocrite mặc kệ truyền máu, hay chèn ép thần kinh đùi. Biện pháp phẫu thuật là hút máu ra và khâu lại ( 7, 9, 10 ) .
Nhiễm trùng vị trí chọc hiếm khi xảy ra ( tỉ lệ khoảng chừng 0,06 – 0,6 % tùy theo đường động mạch quay hay đùi ), nhưng tỷ suất này sẽ tăng lên khi dùng những dụng cụ đóng động mạch đặc biệt quan trọng. Hai dụng cụ thường dùng là Perclose ( Abbott Laboratories, Abbott Park, IL, USA ), một dụng cụ dùng kỹ thuật khâu và Angioseal ( St Jude Medical, St Paul, MN, USA ), một dụng cụ dùng nút chặn collagen. Khi dùng những dụng cụ này sẽ rút ngắn thời hạn nằm trên giường sau PCI ( từ 6 xuống 2 giờ ) và giúp bệnh nhân tự do. Tuy nhiên việc sử dụng dụng cụ đóng sau PCI không cho thấy làm giảm rủi ro tiềm ẩn của biến chứng tại chỗ và việc đưa một vật lạ vào vị trí nhiễm trùng sẽ hoàn toàn có thể gây ra nhiễm trùng tại vị trí chọc. Vi khuẩn thường gặp là staphylococus và cầu khuẩn nhóm B. Các yếu tố tương quan nhiễm trùng là thời hạn thủ pháp lâu, để vỏ ống thông lâu hơn 24 giờ, nhiều ống thông ở một vị trí … Nhiễm trùng vị trí chọc thường phân phối với kháng sinh đường tĩnh mạch, nhưng những bệnh nhân này cũng nên được gởi lại cho những TT tim mạch để bác sĩ ngoại khoa nhìn nhận vì có một số ít trường hợp hoàn toàn có thể dẫn tới vỡ động mạch đùi ( 7,9,10 ) .
Chúng ta khuyên bệnh nhân nên tránh những hoạt động giải trí mạnh và mang vác nặng trong tuần đầu sau can thiệp động mạch vành qua da. Khuyến khích họ tham gia chương trình phục sinh tim mạch tại chỗ để giúp họ từ từ thực thi lại mức độ những hoạt động giải trí của mình với sự tự tin .
Đường động mạch quay thì thuận tiện cho bệnh nhân hơn và ít có rủi ro tiềm ẩn máu tụ, giả phình mạch hay dò động tĩnh mạch. Thỉnh thoảng hoàn toàn có thể mất mạch quay nhưng sẽ không gây ra thiếu máu tay cấp vì đã có tuần hoàn bàng hệ đủ từ động mạch trụ mà đã được nhìn nhận bằng trắc nghiệm Allen trước khi thực thi thủ pháp ( 8 ) .
Nồng độ Creatinin trong máu
Ngày nay những phòng thông tim dùng thuốc cản quang không có ion hóa là những chất dung nạp tốt hơn những thế hệ cản quang cũ. Tuy nhiên, người lớn tuổi, tiểu đường và những bệnh nhân suy thận nhẹ ( creatinine > 1,5 mg % ), người ghép thận thì có rủi ro tiềm ẩn bệnh thận do thuốc cản quang. Nồng độ của creatinine trong huyết thanh sẽ cao nhất vào ngày 1 và 2 sau PCI và thường trở lại thông thường sau 7 ngày mà không cần điều trị đặc hiệu. Tuy nhiên nó hoàn toàn có thể tiến triển đến suy thận tiến trình cuối cần phải lọc thận nếu bệnh nhân đã có công dụng thận kém trước đo ( 11, 12 ). Do vậy, tất cả chúng ta cần theo dõi những bộc lộ suy thận ở bệnh nhân sau PCI trong thời hạn này để có hướng xử trí kịp thời. Tại bệnh viện Nhân dân 115, chúng tôi đã gặp trường hợp bệnh nhân sau làm thủ pháp 2 tuần phải nhập viện lại vì suy thận dù bệnh nhân lúc xuất viện thông thường và đã có biểu lộ triệu chứng một tuần trước đó nhưng không được theo dõi phát hiện. Chúng tôi hiện đang vận dụng những giải pháp phòng ngừa bệnh thận do thuốc cản quang cho đối tượng người dùng rủi ro tiềm ẩn cao gồm có dùng N-acetylcysteine cho ngày trước PCI cùng với truyền đủ dịch và bicarbonate. Bên cạnh đó, giải pháp chính là hạn chế số lượng thuốc cản quang ( thường không quá 3 – 5 ml / kg cho một lần thủ pháp ) ( 7, 11, 12 ) .
Nguyên nhân suy thận khác sau PCI nhưng hiếm khi được chẩn đoán phân biệt với bệnh thận do thuốc cản quang là bệnh thận do mảng xơ vữa gây thuyên tắc. Tỉ lệ gặp khoảng chừng 0,15 %. Nguy cơ cao là xơ vữa lan tỏa hay phình động mạch chủ bụng. Bệnh thận thoái hóa do mảng xơ vữa gây thuyên tắc thường xảy ra sau một quy trình với diễn tiến từ từ và gây suy thận hàng tuần tới hàng tháng sau. Việc phát hiện ra những biến hóa ở da do viêm mạch máu giúp cho chẩn đoán lâm sàng của bệnh thuyên tắc do mảng xơ vữa. Chẩn đoán xác lập bằng sinh thiết thận hay sinh thiết da nhưng thường thì không thiết yếu vì bệnh cảnh lâm sàng thường đủ để chẩn đoán. Đáp ứng với điều trị là rất kém. Nên gửi bệnh nhân lại bác sĩ can thiệp để theo dõi nội trú khi bệnh nhân có biểu lộ ngày càng tăng nồng độ creatinin từ từ và trường diễn ( 13 ) .
Số lượng tiểu cầu
Bệnh giảm tiểu cầu do thuốc là biến chứng hiếm gặp khi dùng heparin ( 1-5 % bệnh nhân dùng heparin không phân đoạn và < 1 % nếu dùng heparin khối lượng phân tử thấp ) và ức chế glycoprotein ( Gp ) IIb / IIIa ( nhiều lúc dùng trong những trường hợp PCI có rủi ro tiềm ẩn cao ). Giảm tiểu cầu do heparin ( HIT ) gồm 3 loại ( phân theo thời hạn ) : HIT nổi bật ( giảm tiểu cầu 5-10 ngày sau dùng heparin ), HIT khởi phát nhanh ( giảm tiểu cầu không Dự kiến trước, thường trong vòng 24 giờ ở những bệnh nhân đã dùng heparin trước đây, thường 2-3 tuần hay thậm chí còn 100 ngày ), HIT trễ ( giảm tiểu cầu và phối hợp với huyết khối 5-19 ngày sau dừng điều trị heparin ). Hậu quả là làm tăng tỉ lệ huyết khối ngay sau khi ngừng heparin. Dấu hiệu lâm sàng gợi ý là ban đỏ hay tổn thương hoại tử da ở chỗ tiêm heparin. Tổn thương này Open > = 5 ngày sau dùng heparin, hay sớm hơn nếu có kháng thể HIT sống sót từ lần dùng trước ( 14 ). Do vậy cần đếm số lượng tiểu cầu sau khi dùng heparin, ức chế Gp IIb / IIIa. Tần suất, thời hạn, xét nghiệm chẩn đoán và điều trị giảm tiểu cầu sau PCI được nêu ở bảng 1 .
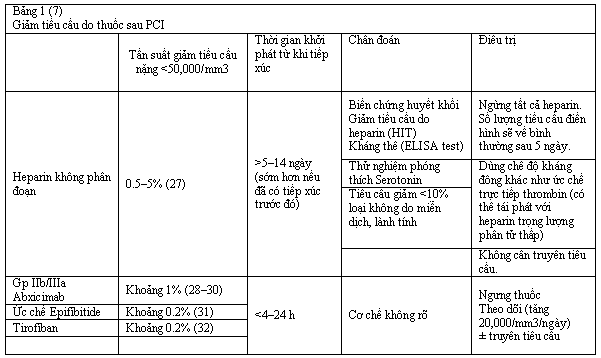
Thông thường heparin không cần dùng sau PCI và thường chỉ truyền tiếp ức chế Gp IIb/IIIa 18 giờ sau PCI trong phần lớn các trường hợp. Những thuốc nêu trên cần ngưng sớm hơn nếu phát hiện giảm tiểu cầu trầm trọng (< 30.000/ mm3) do thuốc. Giảm tiểu cầu do thuốc hiếm khi xảy ra trong cộng đồng vì những thuốc này được ngưng trong vòng 24 giờ và có chế độ theo dõi số lượng tiểu cầu thường qui. Khi có giảm tiểu cầu chúng ta nên tham khảo với bác sỹ tim mạch can thiệp làm thủ thuật chứ không bao giờ được tự ý ngừng clopidogrel và aspirin. Ở bệnh nhân đã có tiền sử HIT, khi can thiệp sẽ dùng các thuốc ức chế thrombin trực tiếp (argatroban, bivalirudin, và lepirudin) thay cho heparin (14, 15). Đánh giá đau ngực sớm sau PCI
Đau ngực sau PCI là một thử thách chung so với những nhà thực hành thực tế y khoa. Trên 50 % bệnh nhân sau can thiệp động mạch vành qua da đôi lúc có đau ngực. Nguyên nhân thì có nhiều từ cảm xúc lành tính sau đặt stent cho tới huyết khối trong stent cấp cực kỳ nguy hại. Do vậy cần hỏi bệnh và khám kỹ bệnh nhân. Điện tâm đồ là bắt buộc trong nhìn nhận đau ngực sớm sau PCI. Những cảm xúc đau ngực ít mà lê dài với một mức độ cố định và thắt chặt từ khi đặt stent với điện tâm đồ thông thường hoàn toàn có thể chỉ nên theo dõi và cần được nhìn nhận lại. Những bệnh nhân có cơn đau thắt ngực nổi bật, đổi khác ECG cần hội chẩn ngay với bác sĩ can thiệp. Những trường hợp đau ngực khác, do cần cẩn trọng với huyết khối trong stent cấp, nên việc nhìn nhận cần được triển khai thận trọng và nên tranh luận với bác sỹ tim mạch can thiệp của bệnh nhân ( Hình 1 ) ( 7, 16 ) .
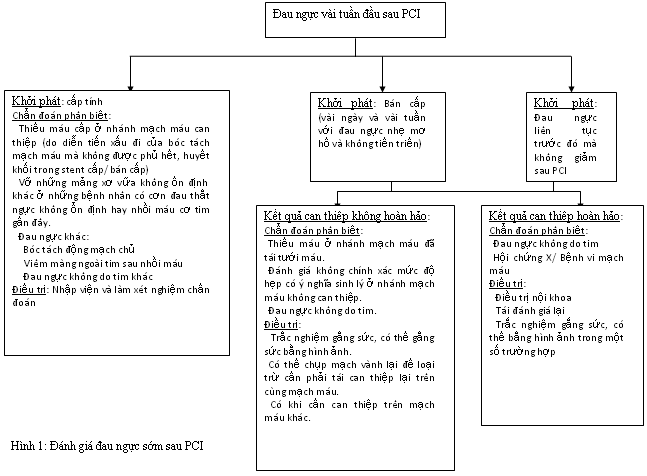
Điều trị trung và dài hạn sau PCI
Vấn đề điều trị lâu dài sau PCI thì rất chuyên biệt và khác nhau trên từng bệnh nhân nhưng nói chung gồm phát hiện và điều trị thiếu máu cục bộ cơ tim tái phát (vai trò của trắc nghiệm gắng sức- TNGS sau PCI), loạn nhịp và suy tim, điều trị đủ thuốc chống kết tập tiểu cầu và phòng ngừa thứ phát (7, 16).
Phát hiện ra thiếu máu cục bộ cơ tim tái phát
Thiếu máu cơ tim tái phát sau PCI hoàn toàn có thể do tái hẹp, tiến triển của bệnh trên cùng mạch vành đã can thiệp hay mạch máu khác, hay ngày càng tăng nhu yếu cơ tim do những nguyên do khác ( 5,6,17 ) .
Lâm sàng nổi bật của tái hẹp thường xảy ra khoảng chừng 3 tháng sau PCI và đạt mức trung bình lúc 12 tháng. Tái hẹp nhanh trong tháng đầu là rất hiếm gặp. Đau ngực xảy ra sau 12 tháng PCI thì gợi ý nhiều tới bệnh xơ vữa mạch vành tiến triển hơn là tái hẹp. Tuy nhiên cũng nên nhớ rằng ngày càng tăng nhu yếu của cơ tim hoàn toàn có thể gây đau ngực sau PCI. Ví dụ, nhu yếu của cơ tim tăng hoàn toàn có thể do thiếu máu hay hẹp van động mạch chủ. Tăng năng lực gắng sức của bệnh nhân sau khi tái lưu thông động mạch ngoại biên vì đau cách hồi cũng hoàn toàn có thể làm tăng nhu yếu của cơ tim ( 7, 17 ) .
Ngoài ra, triệu chứng đau thắt ngực cũng hoàn toàn có thể xảy ra ở bệnh nhân sau tái lưu thông mạch dù không có tổn thương tái hẹp ở cầu nối hay ở đoạn động mạch đã được tái lưu thông. Khoảng 1/3 bệnh nhân tái lưu thông động mạch vành hoàn toàn có thể bộc lộ đau ngực dù không có ùn tắc động mạch rõ ràng. Nguyên nhân của những thực trạng này hoàn toàn có thể như sau ( 5,6 ) :
– Tăng phản ứng mạch máu thượng tâm mạc quá mức ( more intense epicardial coronary vasoreactivity ) ở bệnh nhân sau đặt stent. Điều này thường xảy ra sau một thời hạn đặt stent gây đau thắt ngực muộn. Cần xác lập nguyên do này ở bệnh nhân đau thắt ngực sau can thiệp ( đau thắt ngực không có vùng thiếu máu cục bộ, thường bằng xạ hình tưới máu ) để tránh tái can thiệp không thiết yếu .
– Kết quả PCI không tối ưu, ( suboptimal PCI results ) : Thường xảy ra ở bệnh nhân với tổn thương phức tạp ( type C ) như tổn thương quá dài, huyết khối, vôi hóa, tổn thương chỗ chia nhánh, tắc mạn tính … làm cho hiệu quả thủ pháp không được tuyệt đối .
– Tái thông mạch không trọn vẹn ( incomplete revascularization ) : Ở bệnh nhân tổn thương nhiều nhánh, đôi khi không hề triển khai được tái thông trọn vẹn tổng thể những động mạch bị tổn thương ( những nhánh tổn thương quá nhỏ như đường kính dưới 1,5 mm, hoặc tổn thương quá khó hoặc quá nguy khốn không hề thực thi được … ) và những đoạn động mạch không được tái thông này hoàn toàn có thể là nguyên do làm bệnh nhân đau ngực sau này .
Với việc sử dụng ngày càng nhiều stent phủ thuốc, tỉ lệ tái hẹp đã giảm đáng kể. Do vậy, khác với những nghiên cứu và điều tra trước đây ( đa phần trên bệnh nhân PTCA hoặc đặt stent thường ), những nghiên cứu và điều tra lúc bấy giờ cho thấy chưa có vật chứng làm trắc nghiệm gắng sức thường qui sau PCI là có lợi hơn. Tuy nhiên cần thực thi trắc nghiệm gắng sức thường qui 4-6 tuần sau PCI trên những trường hợp tinh lọc khi có rủi ro tiềm ẩn cao tái hẹp mà ảnh hưởng tác động tới một vùng lớn cơ tim theo như khuyến nghị của hướng dẫn của ACC / AHA ( box 1 ). Các bệnh nhân khác tùy theo có đau ngực hay không mà quyết định hành động kế hoạch chẩn đoán ( hình 2 ). Nếu cần thực thi TNGS nên triển khai TNGS không xâm lấn bằng hình ảnh ( không nên dùng ECG gắng sức ) với độ nhạy cảm và độ đặc hiệu cao hơn ( siêu âm, xạ hình tưới máu hay cộng hưởng từ – MRI ). MSCT 64 lát cắt để phát hiện tái hẹp đang còn nghiên cứu và điều tra. Dưới đây là đề xuất lúc bấy giờ về sử dụng TNGS sau PCI ( 1, 18-20 ) :
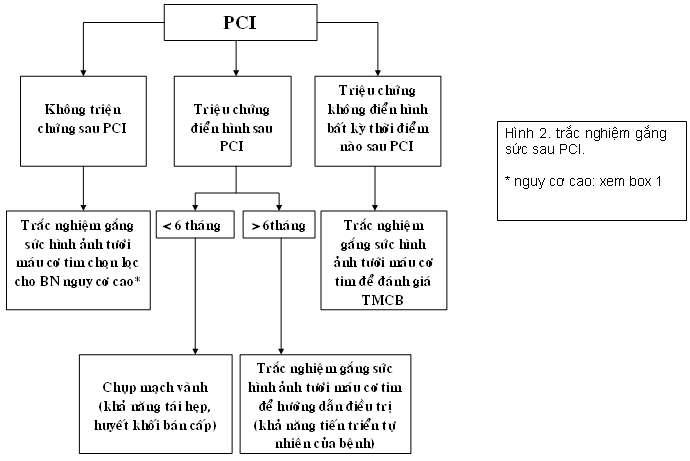
– Bệnh nhân có năng lực gắng sức, triển khai TNGS số lượng giới hạn triệu chứng ( symptom – limited ) bằng xe đạp điện hoặc thảm lăn. Bệnh nhân không có năng lực gắng sức, thực thi TNGS bằng thuốc .
– Bệnh nhân can thiệp thành công xuất sắc, không biến chứng, và không hề đau ngực, không cần thực thi TNGS thường quy ngoại trừ trường hợp rủi ro tiềm ẩn cao đã nêu trên .
– Bệnh nhân có triệu chứng thiếu máu cục bộ cơ tim nổi bật < 6 tháng sau can thiệp ( đặc biệt quan trọng triệu chứng tựa như như trước can thiệp ), nên được chụp lại mạch vành ngay, trừ khi có chống chỉ định. Nếu đau thắt ngực Open muộn > 6 tháng, tất cả chúng ta nên triển khai TNGS hình ảnh cho bệnh nhân để nhìn nhận mức độ và vùng thiếu máu cục bộ .
– Bệnh nhân với triệu chứng không nổi bật nên triển khai TNGS hình ảnh ở bất kể thời gian nào để nhìn nhận xem triệu chứng này có tương quan với thiếu máu cục bộ hay không .
– Trắc nghiệm gắng sức nên trì hoãn vài tuần sau PCI, nhưng nhiều lúc trắc nghiệm gắng sức ( ngay cả một ngày sau khi đặt stent ) hoàn toàn có thể được thực thi mà không có rủi ro tiềm ẩn huyết khối trong stent bán cấp hay những biến chứng mạch máu tại chỗ trên những bệnh nhân được lựa chọn cẩn trọng. Một nguyên do khác để trì hoãn trắc nghiệm gắng sức vài tuần vì trắc nghiệm xạ hình tưới máu cơ tim dương thế giả nếu triển khai quá sớm sau PCI. MRI hoàn toàn có thể triển khai bảo đảm an toàn ngay lập tức sau PCI mà không sợ stent vận động và di chuyển .
Bệnh nhân với tác dụng TNGS hình ảnh âm tính hay dương thế rủi ro tiềm ẩn thấp sau PCI, thực thi lại TNGS này mỗi 2 năm hay khi có triệu chứng. Đối với bệnh nhân đái tháo đường, thời hạn lặp lại nên sớm hơn vì bệnh tiến triển nhanh hơn .
|
Box 1. nhóm bệnh nhân cần trắc nghiệm GS hình ảnh sớm: |
|
• Bệnh nhiều nhánh ĐMV. • LAD đoạn gần, thân chung. • Đột tử trước đây. • Tiểu đường. • Kết quả PCI không tối ưu. • Nghề nguy hiểm. • Giảm chức năng thất trái. |
Chụp mạch vành theo dõi thường qui chỉ được chỉ định trên rất ít trường hợp đặc biệt quan trọng, gồm có những bệnh nhân được đặt stent ở thân chung động mạch vành trái. Những trường hợp này chụp mạch vành lại hoàn toàn có thể được triển khai trong vòng 3-9 tháng sau can thiệp ( 7 ) .
Thời gian dùng chế độ hai thuốc chống kết tập tiểu cầu
Huyết khối trong stent là yếu tố làm đau đầu những nhà tim mạch can thiệp. Huyết khối trong stent được phân loại dựa theo thời hạn Open huyết khối trong stent ( box 2 ) ( 21 ). Biến chứng này tuy hiếm nhưng rõ ràng là dẫn đến những hậu quả nặng nề gồm có nhồi máu cơ tim và đột tử. Tần suất chung là dưới 1 % nếu dùng chính sách hai thuốc chống kết tập tiểu cầu và kỹ thuật đặt stent với áp lực đè nén cao. Đa số trường hợp xảy ra sớm sau đặt stent. Cơ chế hình thành huyết khối tuỳ thuộc vào huyết khối trong stent sớm hay trễ. Huyết khối sớm thường tương quan đến những yếu tố cơ học tích hợp với đặt stent gồm có tổn thương mạch máu, đường kính lòng mạch nhỏ và / hoặc lưu lượng dòng máu chậm sau đặt stent. Ngược lại, chính sách của huyết khối trong stent trễ với DES là do làm chậm hay không trọn vẹn quy trình nội mạc hóa. Một vài trường hợp đã được báo cáo giải trình có huyết khối trong stent rất trễ ( hơn 12 tháng sau đặt stent ) trong vòng những ngày ngưng dùng thuốc chống kết tập tiểu cầu khi bệnh nhân được đặt stent phủ thuốc ( DES ) ( 1, 7, 21 ). Chế độ hai thuốc chống kết tập tiều cầu gồm aspirin với clopidogrel do đó là khởi đầu bắt buộc so với những bệnh nhân được đặt stent mạch vành ( 22-24 ) .
|
Box 2. phân loại huyết khối. Sớm : |
Hiệu quả của chính sách hai thuốc chống tiểu cầu trong giảm huyết khối cấp và bán cấp trong stent đã được xác lập rõ. Tuy nhiên thời hạn tối ưu của chính sách hai thuốc chống kết tập tiểu cầu để dự trữ huyết khối muộn trong stent còn chưa thống nhất. Quan niệm lúc bấy giờ là 4 tuần so với stent bằng sắt kẽm kim loại, trong vòng tối thiểu một năm so với DES. Trong những trường hợp đăc biệt dùng nhiều stent DES phủ chồng lên nhau hay đặt stent phủ thuốc ở thân chung khuyến nghị dùng hai thuốc chống kết tập tiểu cầu hoàn toàn có thể lâu hơn hoặc không hạn định ( 2, 15, 22-24 ). Bảng 2 tóm tắt đề xuất dùng hai thuốc chống tiểu cầu lúc bấy giờ .
|
Bảng 2. Cập nhật hướng dẫn PCI 2007 về dùng 2 thuốc chống tiểu cầu (2). |
|
Class I 1. Bệnh nhân đang uống dài hạn aspirin phải uống aspirin 75-325 mg trước can thiệp . 2. Bệnh nhân chưa uống aspirin phải uống 325 mg tối thiểu 2 giờ trước can thiệp ( lý tưởng trước 24 giờ ) 3. Sau PCI, ở bệnh nhân không dị ứng hay rủi ro tiềm ẩn chảy máu cao, phải uống 162 – 325 mg / ngày aspirin liên tục trong 1 tháng so với stent thường, 3 tháng so với stent phủ sirolimus, 6 tháng với stent phủ parlitaxel. Sau đó uống dài hạn aspirin với liều 75-162 mg / ngày . 4. Liều nạp clopidogrel, nhìn chung là 600 mg trước hay khi thưc hiện can thiệp. Ở bệnh nhân dùng tiêu sợi huyết trong vòng 12-24 giờ, liều nạp nên chỉ là 300 mg . 5. Sau can thiệp, dùng clopidogrel tối thiểu 1 năm cho trường hợp dùng stent phủ thuốc nếu không có rủi ro tiềm ẩn chảy máu. Dùng tối thiểu 1 tháng cho trường hợp stent thường và lý tưởng là tới 12 tháng ( trừ khi bệnh nhân có rủi ro tiềm ẩn chảy máu cao, khi đó hoàn toàn có thể cho tối thiểu 2 tuần ) . Class IIa 1. Ở bệnh nhân rủi ro tiềm ẩn chảy máu cao, dùng liều aspirin thấp hơn ( 75-162 mg / ngày ) trong quy trình tiến độ đầu sau can thiệp . Class IIb 1. Quan tâm sử dụng clopidogrel dài hạn cho trường hợp dùng stent phủ thuốc . |
Dùng Warfarin sau PCI
Kháng đông đường uống như warfarin, ngay cả khi tích hợp với aspirin, thì có hiệu suất cao thấp hơn chính sách hai thuốc chống kết tập tiểu cầu trong tính năng ngăn ngừa huyết khối trong stent cấp. Tuy nhiên, warfarin la # bắt buộc cho một số ít bệnh nhân ví dụ bệnh nhân có van tim cơ học, rung nhĩ rủi ro tiềm ẩn cao hay những chỉ định khác của warfarin. Đối với những bệnh nhân này, có thời gian phải dùng 3 thuốc chống đông. Đây thực sự là một yếu tố trong thực hành thực tế lâm sàng. Các số liệu về yếu tố này còn hạn chế và đang biến hóa. Cách điều trị tối ưu sau PCI nên được kiểm soát và điều chỉnh theo từng bệnh nhân nhờ vào vào việc giám sát rủi ro tiềm ẩn thuyên tắc huyết khối và huyết khối trong stent với rủi ro tiềm ẩn chảy máu do dùng khá đầy đủ chính sách hai thuốc chống kết tập tiểu cầu với warfarin. Nếu phải sử dụng 3 thuốc, liều asprin là 75-81 mg, clopidogrel là 75 mg, duy trì INR 2,0 – 2,5. Những bệnh nhân rủi ro tiềm ẩn chảy máu cao ( > 75 tuổi, tiền căn xuất huyết não … ) nên đặt stent thường ( phủ carbon hay heparin … ) hoặc phẫu thuật và không nên triển khai chính sách 3 thuốc kháng đông này. Nên cho thuốc ức chế bơm proton để bảo vệ dạ dày ở toàn bộ bệnh nhân ( 22-24 ). Bảng 3 ra mắt những bệnh cảnh lâm sàng mẫu và cách điều trị .
|
Bảng 3 (7) Chế độ điều trị đề nghị cho những bệnh nhân can thiệp mạch vành qua da mà có kèm chỉ định dùng warfarin |
|
| Tình huống lâm sàng | Điều trị ý kiến đề nghị |
| Bệnh van tim cơ học | Warfarin liên tục suốt đời |
| Rung nhĩ và “ rủi ro tiềm ẩn thuyên tắc do huyết khối cao ” ( như bệnh van hai lá hậu thấp và tiền căn tai biến mạch máu não ) |
VÀ Aspirin và clopidogrel 4 tuần và ngưng ( BMS ) |
| Rung nhĩ và “ rủi ro tiềm ẩn thuyên tắc do huyết khối trung bình ” ( như bệnh nhân lớn tuổi tiểu đường tăng huyết áp ) |
Dùng như Rung nhĩ và “nguy cơ thuyên tắc do huyết khối cao” như trên |
|
HAY |
|
| Aspirin và clopidogrel 4 tuần, rồi chuyển qua warfarin ( BMS ) | |
| Aspirin và clopidogrel 3-6 tháng, rồi chuyển clopidogrel qua warfarin. Chỉ dùng warfarin sau 12 tháng ( DES ) | |
| Nếu rủi ro tiềm ẩn chảy máu cao, chỉ dùng warfarin sau 4 tuần ( nên xem xét đặt stent sắt kẽm kim loại thường ở nhóm bệnh nhân này ) | |
|
HAY |
|
| Aspirin và clopidogrel suốt đời ( Nghiên cứu ACTIVE có tác dụng vào 2007 sẽ đưa ra Kết luận về yếu tố này ) | |
| Rung nhĩ và “ rủi ro tiềm ẩn thuyên tắc do huyết khối thấp ” ( như bệnh nhân lớn tuổi có rung nhĩ đơn độc ) | Giống chính sách hai thuốc chống tiểu cầu . |
Chảy máu sau PCI với các thuốc chống kết tập tiểu cầu và warfarin
Trong nghiên cứu và điều tra CURE, tần suất chảy máu quan trọng trong 30 ngày với chính sách hai thuốc chống kết tập tiểu cầu ( 1.7 % ) là cao hơn khi so sánh với dùng aspirin đơn độc ( 1.1 % ). Tuy nhiên, chính sách 2 thuốc này không làm tăng thêm rủi ro tiềm ẩn chảy máu gây tử trận hay đột quỵ do xuất huyết. Nguy cơ chảy máu khi dùng hai thuốc riêng không liên quan gì đến nhau trong điều tra và nghiên cứu CAPRIE là 1.55 % so với aspirin và 1.38 % so với clopidogrel trong vòng 1 năm. Dù số liệu còn hạn chế, nhưng cho thấy chính sách 3 thuốc ( aspirin, clopidogrel với warfarin ) sẽ có rủi ro tiềm ẩn chảy máu cao ( 9.2 % ) hơn là warfarin với aspirin ( 6.5 % ) ( 7 ) .
Điều trị chảy máu cấp ( 25 ) :
– Nếu chảy máu xảy ra ở bệnh nhân sau mổ mà không ngưng thuốc chống tiểu cầu, phải ngưng ngay những thuốc này. Nguyên tắc điều trị chảy máu nặng giống như thường thì, gồm có truyền dịch, truyền hồng cầu lắng, và điều trị ngọai khoa hay những giải pháp cầm máu khác bất kể khi nào thiết yếu .
– Nếu chảy máu ở đường tiêu hóa và có năng lực cầm máu bằng nội soi hay biệp pháp cơ học khác, thực thi cầm máu ngay và không cần phải ngưng những thuốc chống tiểu cầu, đặc biệt quan trọng ở bệnh nhân rủi ro tiềm ẩn huyết khối cao .
Ngưng tạm thời thuốc chống tiểu cầu
Đôi khi bệnh nhân phải trải qua thủ pháp sau khi đặt stent. Khi đó yếu tố đặt ra là liên tục hay ngưng hàng loạt hay một phần thuốc chống tiểu cầu ? Quyết địng này dựa trên xem xét giữa rủi ro tiềm ẩn chảy máu của thủ pháp hay phẫu thuật và rủi ro tiềm ẩn huyết khối của bệnh nhân. Chiến lược điều trị thuốc chống tiều cầu để hạn chế rủi ro tiềm ẩn huyết khối trong stent quanh thủ thuật gồm có ( 25,26 ) :
– ( 1 ) Tiếp tục hai thuốc chống tiểu cầu trong và sau thủ pháp. Chiến lược này đặc biệt quan trọng dùng cho bệnh nhân trải qua phẫu thuật sớm sau đặt stent ( rủi ro tiềm ẩn huyết khối cao ). Cần tìm hiểu thêm những phẫu thuật viên để lượng giá rủi ro tiềm ẩn chảy máu của thủ pháp, qua đó xem xét giữa quyền lợi và rủi ro tiềm ẩn của việc dùng thuốc. Những thủ pháp hoàn toàn có thể cầm máu tại chỗ như nhổ răng, phẫu thuật da, thủy tinh thể hoàn toàn có thể không cần ngưng thuốc chống tiểu cầu .
– ( 2 ) Ngừng thuốc clopidogrel và chuyển dùng thuốc chống tiểu cầu tính năng ngắn hay thuốc chống đông. Thuốc thường dùng là ức chế glycoprotein IIb / IIIa hay antithrombin, và dùng lại clopidogrel càng sớm càng tốt sau phẫu thuật. Chiến lược này thường dùng khi phải phẫu thuật sớm sau đặt stent và cần phải ngưng clopidogrel .
– ( 3 ) Ngừng clopidogrel và dùng lại sau phẫu thuật. Chiến lược này dùng khi stent được nghĩ là đã nội mạc hóa vừa đủ và rủi ro tiềm ẩn huyết khối rất thấp. Các bệnh nhân trải qua phẫu thuật thần kinh cũng nên theo kế hoạch này vì rủi ro tiềm ẩn chảy máu cao. Khi dùng lại thuốc, nên dùng liều nạp 600 mg clopidogrel .
Bảng 4 dưới đây tóm tắt những đề xuất của hội hồi sức và gây mê của Pháp về kế hoạch điều trị thuốc chống tiều cầu ở bệnh nhân dặt DES phải trải qua phẫu thuật .
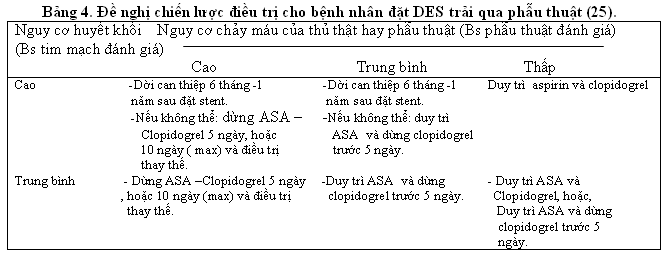
Phòng ngừa thứ phát sau PCI
Tuân thủ theo những hướng dẫn lúc bấy giờ ( bỏ thuốc lá, hoạt động thể lực đều, giảm cân, trấn áp tốt HA, rối loạn mỡ máu, đường huyết … ) ( 3 ). Đề nghị tìm hiểu thêm thêm những tài liệu hướng dẫn dự trữ thứ phát vì phần này không phải là mục tiêu chính của bài viết này .
Tiên lượng
Tiên lượng của những bệnh nhân được tái lưu thông mạch máu trọn vẹn, không thay đổi và tính năng thất trái bảo tồn nói chung tốt. Ở những bệnh nhân trẻ ( < 60 tuổi ) không tiểu đường với 1 nhánh mạch vành và công dụng thất trái tốt, tiên lượng vĩnh viễn sau PCI tương tự như như dân số chung ( 7 ). Trong nghiên cứu và điều tra sổ bộ ARTS II vừa được công bố gần đây ( 27 ) cho thấy PCI dùng stent phóng thích sirolimus trong bệnh đa mạch máu đạt được tỷ suất sống còn không biến cố trong 1 năm tương tự với mổ bắc cầu trong điều tra và nghiên cứu ARTS I ( 28 ) . Tuy nhiên có một nhóm nhỏ của bệnh nhân sau PCI vẫn còn công dụng thất trái kém mặc dầu đã được tái lưu thông mạch máu. Những bệnh nhân có triệu chứng suy tim NYHA III tới IV có tỷ suất tử trận hàng năm từ 20-50 %. Đột tử chiếm trên phân nửa số tử trận này ( 7 ) .
Điều trị loạn nhịp ác tính và suy tim sau PCI
Những bệnh nhân loạn nhịp và suy tim nên gởi cho bác sỹ tim mạch hay bác sỹ có kinh nghiệm tay nghề về chăm nom tim mạch .
Những thuốc chống loạn nhịp nên dùng thận trọng ở những bệnh nhân có bệnh mạch vành và rối loạn tính năng thất trái. Ức chế Bêta là thuốc lựa chọn tiên phong do tính năng chống loạn nhịp của nó và đã được chứng tỏ có quyền lợi trong cải tổ tỷ suất tử trận so với bệnh nhân suy tim ( 29,30 ). Những thuốc chống loạn nhịp nhóm I ( flecainide và propafenone ) là chống chỉ định ( 31,32 ). Amiodarone thì bảo đảm an toàn khi dùng cho những bệnh nhân suy tim NYHA II nhưng không có quyền lợi trên tỷ suất tử trận ( 33 ) .
Tất cả những bệnh nhân sau PCI đều có chỉ định của thuốc ức chế men chuyển. Lợi ích của nhóm ức chế men chuyển đã được xác lập rõ ràng trên bệnh nhân suy thất trái ( 34 ). Ngay cả những bệnh nhân có phân suất tống máu thất trái còn bù trừ thì quyền lợi của nhóm ức chế men chuyển là làm giảm tỷ suất những biến cố tim mạch ( 35 ). Nhóm ức chế thụ thể angiotensin II cũng nên được xem xét khi bệnh nhân không dung nạp với nhóm Ức chế men chuyển ( 36 ) .
Việc phối hợp nhóm ức chế men chuyển và nhóm ức chế thụ thể angiotensin II điều trị cho những bệnh nhân có phân suất tống máu < 40 % hoàn toàn có thể làm giảm tỷ suất tử trận do tim mạch và tỷ suất tái nhập viện ( 37 ) .
Chẹn Aldosterone với spironolactone hay eplerenone liều thấp cần được xem xét cho những bệnh nhân sau can thiệp có triệu chứng suy tim độ III hay IV do rối loạn công dụng tâm thu thất trái, đặc biệt quan trọng sau nhồi máu cơ tim, với điều kiện kèm theo tính năng thận và nồng độ kali trong máu được theo dõi sát ( 38, 39 ) .
Dung cụ điều trị hỗ trợ cho bệnh nhân sau PCI
Những bệnh nhân sau can thiệp có rối loạn tính năng thất trái do thiếu máu cục bộ không hồi sinh nên được xem xét cấy máy phá rung như phòng ngừa thứ phát cho những bệnh nhân sống sót sau ngừng tim và gần đột tử ( 40,41 ) hay là như phòng ngừa tiên phát nếu phân suất tống máu thất trái nhỏ hơn 30-35 % ( 42,43 ). Tất cả những nghiên cứu và điều tra cấy máy phá rung phòng ngừa tiên phát đều vô hiệu những bệnh nhân không không thay đổi trong thời hạn triển khai ghiên cứu, gồm cả những bệnh nhân trong vòng 2 tháng sau nhồi máu cơ tim và những bệnh nhân có triệu chứng suy tim sung huyết không không thay đổi. Do vậy, sau khi tổng thể những nguyên do gây rối loạn nhịp thất đã được không thay đổi, cần nhìn nhận lại phân suất tống máu thất trái của bệnh nhân sau PCI và năng lực hoàn toàn có thể cấy máy phá rung ( 7 ). Những bệnh nhân sau PCI có những triệu chứng suy tim NYHA III-IV mặc dầu đã được điều trị nội khoa tối ưu nên xem xét điều trị tái đồng nhất tim với đặt máy tạo nhịp hai buồng thất nếu có vật chứng không đồng nhất cơ học hai thất. Trước đây, tín hiệu gợi ý mất đồng nhất cơ học là phức bộ QRS rộng trên điện tâm đồ. Hiện nay kỹ thuật hình ảnh siêu âm kỹ thuật cao giúp phát hiện sự mất đồng điệu và để lựa chọn những bệnh nhân hoàn toàn có thể phân phối tốt với điều trị tái đồng nhất thất ( 44 ) .
KẾT LUẬN
Điều trị bệnh nhân sau PCI không nên chỉ quan tâm đơn thuần là một yếu tố tim mạch. Bệnh xơ vữa động mạch vành không hề chữa khỏi đơn thuần chỉ bằng một giải pháp điều trị. PCI cũng chỉ là một trong nhiều giải pháp điều trị bệnh động mạch vành, không phải không có biến chứng và có hiệu suất cao suốt đời. Do vậy, theo dõi bệnh nhân lâu dài hơn, điều trị thuốc và kiểm soát và điều chỉnh những yếu tố nguy cơ tim mạch cho mọi bệnh nhân sau PCI là bắt buộc. Việc thông tin qua lại giữa bác sỹ tim mạch của bệnh nhân và những bác sỹ nội khoa khác là rất là thiết yếu. Các bác sĩ tim mạch và nội khoa chung nên biết những nguyên tắc cơ bản trong theo dõi và điều trị bệnh nhân sau PCI để giúp bệnh nhân đạt hiệu suất cao điều trị cao nhất, phát hiện sớm nhất những biến chứng và xử trí kịp thời nếu nó xảy ra .
Tài liệu tham khảo
1. AHA / ACC / SCAI 2005 guideline update for Percutaneuos Coronary Intervention .
2. 2007 focus update of the AHA / ACC / SCAI 2005 guideline update for Percutaneuos Coronary Intervention .
3. 2007 chronic angina focused update of AHA / ACC 2002 guideline for management of patient with chronic stable angina .
4. AHA. Heart Disease and Stroke Statistics – 2005 Update. Dallas, TX : AHA, 2004 .
5. Lemos. P.A et al : recurrent angina after revascularization : an emerging problem foe the clinician. Coronary artery disease 2004, 15 ( suppl 1 ) : S11-15 .
6. Nguyễn thanh Hiền : đau ngực tái phát sau tái thông mạch. Thới sự tim mạch học .
7. Chan.M et al: a review of the management of patients after PCI. Int J Clin Pract 2006, 60,5, 582-589.
8. Agostoni P, Biodi-Zoccai GG, de Benedictis ML et al. Radial versus femoral approach for percutaneous coronary diagnostic and interventional procedures ; systematic overview and meta-analysis of randomized trials. J Am Coll Cardiol 2004 ; 44 : 349 – 56 .
9. Levine. G.N. and Kern. M.J : Complications of PCI. In Kern. M.J : The interventional cardiac catheterization hanbook. 2 th 2004. p : 162 – 193 .
10. Carrozza. J.P : Periprocedural complications of PCI. Uptodate. 15.2. 2007 .
11. Rudnick. M.R et al : Pathogenesis, clinical features, and dianosis of radiocontrast media-induced acute renal failure. Uptodate 15.2. 2007
12. Davidson C, Hlatky M, Morris K. Cardiovascular and renal toxicity of a nonionic radiocontrast agent after cardiac catheterization. Ann Intern Med 1989 ; 110 : 119 – 20 .
13. Tunick. P.A : Clinical characteristis of renal artheroemboli. Uptodate 15.2. 2007 .
14. Frame. J.N et al : heparin-induced thrombocytopenia and PCI. Cardiology special edition 2004, vol 10 : 24-30 .
15. Hamdalla. H, Steinhubl. S.R : role of platelet inhibitor agents in percutaneous coronary intervention. In Topol. E.J : textbook of interventional cardiology. 5 th 2008 ; p : 147 – 164 .
16. . Kern. M.J Medical therapy after PCI. In Kern. M.J : The interventional cardiac catheterization hanbook. 2 th 2004. p : 67-69 .
17. Costa. M.A, Simon. D.I : Restenosis. In Topol. E.J : textbook of interventional cardiology. 5 th 2008 ; p : 567 – 587 .
18. Papaioannou. G.I et al : Role of stress testing after coronary revascularization. Uptodate 15.2. 2007 .
19. Gerber. T.C, Manning. W.J : noninvasive coronary arteriography with cardiac computer tomography and cardiovascular manegtic resonance. Uptodate 15.2, 2007 .
20. Roffi M, Wenaweser P, Meier B et al. Early exercise after coronary stenting is safe. J Am Coll Cardiol 2003 ; 42 : 1569 – 73 .
21. Barvy. A.A : late stent thrombosis. In Topol. E.J : textbook of interventional cardiology. 5 th 2008 ; p : 549 – 566 .
22. Chew. D.P : anticoagulation in percutaneous coronary. In Topol. E.J : textbook of interventional cardiology. 5 th 2008 ; p : 164 – 182 .
23. Rubboli. A, Verheugt. F.W.A : antithrombotic treatment for patients on oral anticoagulation undergoing coronary stenting. Int J of cardio 2007 : 1/5 .
24. Cutlip. D, Levin. T : antithrombotic therapy for intracoronary stent implantation : recommendations. Uptodate 15.2, 2007 .
25. Bertrand. M.E : when and how to discontinue antiplatelet therapy. Eur Heart J. 2008 ( suppl A ) : A 35 – A 41 .
26. Brilakis. E.S et al : perioperative management of patients with coronary stent. JACC 2007, 49 : 2145 – 2150 .
27. Serruys PW. Arterial Revascularization Therapies Study Part II : Sirolimus-eluting stents for the treatment of patients with multivessel de novo coronary artery lesions. American College of Cardiology 2005 Annual Scientific Session .
28. Packer M, Bristow MR, Cohn JN et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. U S Carvedilol Heart Failure Study Group. N Engl J Med 1996 ; 334 : 1349 – 55 .
29. CIBIS-II Investigators. The Cardiac Insufficiency Bisoprolol Study II ( CIBIS-II ) : a randomized trial. Lancet 1999 ; 353 : 9-13 .
30. MERIT-HF Study Group. Effect of metoprolol CR / XL in chronic heart failure : Metoprolol CR / XL Randomised Intervention Trial Congestive Heart Failure ( MERIT-HF ). Lancet 1999 ; 353 : 2001 – 7 .
31. The Cardiac Arrhythmia Suppression Trial ( CAST ) Investigators. Effect of encainide and flecainide on mortality in a randomized trial of arrhythmia suppression after myocardial infarction. N Engl J Med 1989 ; 321 : 406 – 12 .
32. Kuck KH, Cappato R, Siebels J et al. Randomised comparison of antiarrhythmic drug therapy with implantable defibrillators in patients resuscitated from cardiac arrest. The Cardiac Arrest Study Hamburg ( CASH ). Circulation 2000 ; 102 : 748 – 54 .
33. Brady GH, Lee KL, Mark DB et al. SCD-HeFT Investigators. Amiodarone or an implantable cardioverter defibrillator for congestive heart failure. N Engl J Med 2005 ; 352 : 225 – 37 .
34. Yusuf S, Sleight P, Pogue J et al. The Heart Outcomes Prevention Evaluation ( HOPE ) Study Investigators. Effects of an angiotensinconverting – enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. N Engl J Med 2000 ; 342 : 145 – 53 .
35. The European Trial On Reduction of Cardiac Events with Perindopril in Stable Coronary Artery Disease Investigators. Efficacy of perindopril in the prevention of cardiovascular events among patients with stable coronary artery disease : randomized, double-blind, placebo-controlled, multicentre trial ( the EUROPA study ). Lancet 2003 ; 362 : 782 – 8 .
36. Granger C, McMurray J, Yusuf S et al. The CHARM Investigators. Effects of candesartan in patients with chronic heart failure and reduced left-ventricular systolic function intolerant to angiotensinconverting – enzyme inhibitors : the CHARM-Alternative trial. Lancet 2003 ; 362 : 772 – 6 .
37. McMurray J, Ostergren J, Swedberg K et al. The CHARM Investigators. Effects of candesartan in patients with chronic heart failure and reduced left-ventricular systolic function taking angiotensin – converting-enzyme inhibitors : the CHARM-Added trial. Lancet 2003 ; 362 : 767 – 71 .
38. Pitt B, Zannad F, Remme W et al. Randomised Aldactone Evaluation Study Investigators. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. N Engl J Med 1999 ; 341 : 709 – 17 .
39. Pitt B, Remme W, Zannad F et al. Eplerenone Post-acute Myocardial Infarction Heart Failure Efficacy and Survival Study Investigators. Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med 2003 ; 348 : 1309 – 21 .
40. The Antiarrhythmics Versus Implantable Defibrillators ( AVID ) Investigators. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhythmias. N Engl J Med 1997 ; 337 : 1576 – 83 .
41. Connolly SJ, Gent M, Roberts RS et al. Canadian implantable defibrillator study (CIDS): a randomized trial of the implantable cardioverter defibrillator against amiodarone. Circulation 2000; 101: 1297-302.
42. Moss AJ, Hall WJ, Cannon DS et al. Multicenter Automatic Defibrillator Implantation Trial Investigators. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. N Engl J Med 1996 ; 335 : 1933 – 40 .
43. Moss AJ, Zareba W, Hall WJ et al. Multicenter Automatic Defibrillator Implantation Trial Investigators. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002 ; 346 : 877 – 83 .
44. Yu CM, Zhang Q, Fung JW et al. A novel tool to assess systolic asynchrony and identify responders of cardiac resynchronization therapy by tissue synchronization imaging. J Am Coll Cardiol 2005 ; 45 : 677 – 84 .
Source: http://139.180.218.5
Category: Thuật ngữ đời thường
